| Université d'Angers - Bioénergétique & enzymologie - Session de Juin 2005 |
|
Exercice n°1 (4 points) - Répondre par vrai ou faux aux assertions 1 à 4. |
| A1. L'énergie libre de Gibbs est la partie "utilisable" par la cellule de l'énergie totale d'un processus thermodynamique. | VRAI |
| A2. Une valeur d'énergie libre de Gibbs nulle signifie que la réaction considérée n'est pas à l'équilibre. | FAUX |
| A3. Toutes les réactions du métabolisme sont exergoniques. | FAUX |
| A4. Une enzyme modifie l'énergie libre de Gibbs de la réaction qu'elle catalyse. | FAUX |
|
Exercice n°2 (6 points) - Donner une réponse simple aux questions 1 à 6. |
| Q1. Donnez un exemple de travail cellulaire lié à l'hydrolyse de l'ATP. | mécanique / transport / chimique |
| Q2. Comment s'appelle la liaison entre les groupements phosphoryle en position β et γ de l'ATP ? | phosphoanhydride |
| Q3. Citez un composé dont l'hydrolyse est plus exergonique que celle de l'ATP ? | PEP / créatine phosphate |
| Q4. Comment s'appelle la structure par laquelle transite un substrat avant d'être transformé en produit ? | état de transition |
| Q5. Quelle conséquence cela a-t-il de mesurer la vitesse initiale d'une réaction enzymatique en ce qui concerne le produit ? | sa concentration est négligeable |
| Q6. Sur quelle forme d'une enzyme un inhibiteur compétitif se fixe-t-il ? | forme libre |
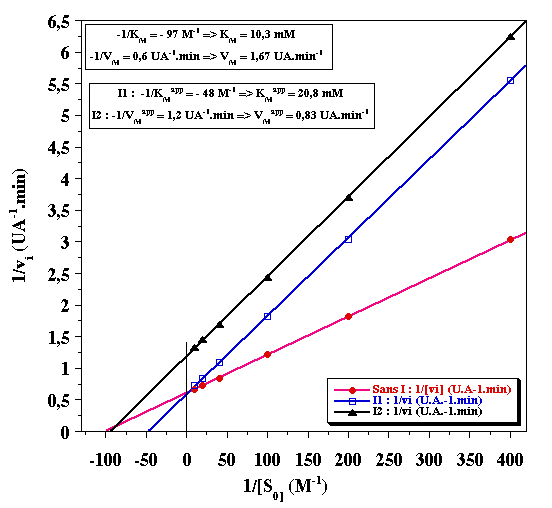
| Exercice n°3 (10 points) |
| paramètres | sans I | I1 | I2 |
-1/VM (UA-1.min) ou -1/VMapp (UA-1.min) |
0,6 | 0,6 | 1,2 |
VM (UA.min-1) ou VMapp (UA.min-1) |
1,67 | 1,67 | 0,83 |
VM (M.min-1) ou VMapp (M.min-1) |
1 10-4 | 1 10-4 | 0,5 10-4 |
kcat (s-1) |
167 | ------- | ------- |
-1/KM (M-1) ou -1/KMapp (M-1) |
- 97 | - 48 | - 97 |
KM (mM) ou KMapp (mM) |
10,3 | 20,8 | 10,3 |
Type inhibition |
------- | compétitif | non compétitif |
| KI (M) | ------- | 2 10-5 | 0,02 |
 |