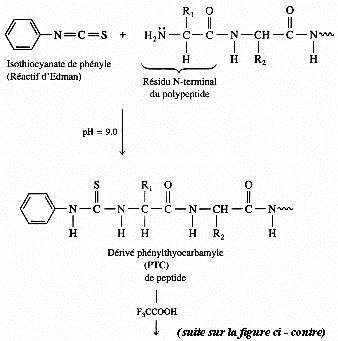
La fonction α-aminée de l'acide aminé en position N-terminale de la chaîne polypeptidique d'une protéine (ou d'un polypeptide) est traitée à pH alcalin par l'isothiocyanate de phényle (PITC), appelé aussi réactif d'Edman.
On obtient un dérivé phénylthiocarbamyle (PTC) de la protéine ou du peptide. Ce dérivé est traité par un acide anhydre tel que l'acide trifluoroacétique.
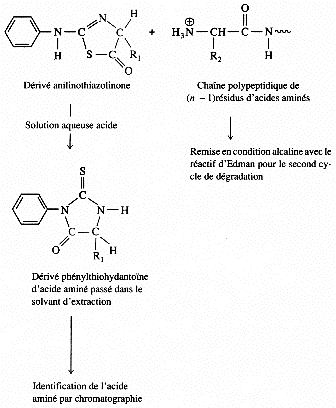
La liaison peptidique liant l'acide aminé en position N-terminale est spécifiquement coupée. Le dérivé anilinothiazolinone de cet acide aminé est séparé du reste de la chaîne polypeptidique par extraction avec un solvant organique, le chlorure de butyle.
On traite ce dérivé instable par une solution acide qui le transforme en dérivé stable : le phénylthiohydantoïne acide aminé (PTH - acide aminé). Le PTH - acide aminé est séparé, quantifié et identifié par chromatographie en phase reverse avec une phase stationnaire sur laquelle est greffée une chaîne alkylée en C18 (octadécyl) ;
Le reste de la chaîne polypeptidique subit de nouveau l'ensemble du traitement et les acides aminés sont ainsi séquencés tour à tour à partir de l'extrémité N-terminale.
Source des figures : "Principes de Biochimie" Horton, Moran, Ochs, Rawn et Scrimgeour (1994), Ed. DeBoeck Universités
Voir une application à l'analyse des acides aminés de Pisum sativum.