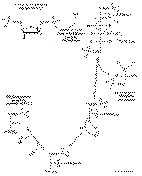
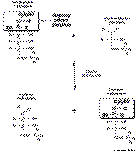2a. On étudie la réaction catalysée par l'aldolase. Ecrire cette réaction et le mécanisme catalytique.
2b. Cette réaction s'accompagne d'une variation d'énergie libre standard physiologique de + 5,79 kcal/mol. Dans les conditions standard, cette réaction va-t-elle dans le même sens que celui dans lequel elle se déroule au cours de la glycolyse ?
In vivo les concentrations du substrat et des produits sont les suivantes :
- [D-fructose 1,6-diphosphate]φ = 31 µM ;
- [D-glycéraldéhyde 3-phosphate]φ = 18,5 µM ;
- [dihydroxyacétone phosphate]φ = 138 µM
- Les conditions de concentrations in vivo sont-elles voisines des conditions de concentration à l'équilibre ?
- Ceci explique-t-il pourquoi le flux global de la glycolyse va dans le sens de la formation du pyruvate ?
Données : T = 37°C ; R = 8,31 -1.K-1 = 1,99 cal.mol-1.K-1
2c. L'aldolase peut catalyser la réaction réverse (formation de l'hexose). Dans ce cas, elle utilise spécifiquement la DHAP, mais elle peut accepter divers D-aldoses. Par ailleurs, la transaldolase catalyse le transfert du groupement dihydroxyacétone (qui correspond aux atomes 1 à 3 du D-sédoheptulose 7-phosphate) sur le G3P.
Quels sont les métabolites présents à l'équilibre aprés incubation de D-fructose 1,6-diphosphate et de D-sédoheptulose 7-phosphate avec l'aldolase et la transaldolase ?