Université d'Angers - Biochimie métabolique - Mars 2015
Question n°1 (10 points) Répondre par VRAI ou FAUX aux assertions suivantes.
| A1. Si A = 1, l = 1 cm et εM = 1 M-1.cm-1, alors C = 0,1 M. | FAUX |
| A2. La variation d’énergie libre de Gibbs quantifie la chaleur récupérée lors d’un processus biologique. | FAUX |
| A3. L’ATP est la molécule universelle de l’énergie et l’un des 4 nucléotides de l’ADN. | FAUX |
| A4. Si C = 0,1 M, l = 1cm et εM = 1 M-1.cm-1, alors A = 0,1. | VRAI |
| A5. 180 mg de BSA (MM = 6,64 104 g.mol-1) dans 0,1 L, alors [BSA] = 2,7 mM. | FAUX |
| A6. Si ΔG0' = - 1 kJ/mol, T = 10°C, R = 8,31 J.mol-1.K-1, alors Keq = 15,3. | FAUX |
| A7. Les coenzymes sous forme oxydée (NAD+ et FAD) représentent une source d’énergie. | FAUX |
| A8. La grande majorité des réactions de la glycolyse se déroulent au voisinage de l’équilibre. | VRAI |
| A9. Le dATP est la molécule universelle de l’énergie et l’un des 4 nucléotides des ARN. | FAUX |
| A10. La chaine latérale de G est : -COOH. | FAUX |
| A11. Toutes les protéines marquées par l’ubiquitine sont destinées à la dégradation par un protéasome. | FAUX |
| A12. Le KM élevé de la glucokinase pour le glucose permet que le foie stocke celui-ci sous forme de glycogène quand le taux de glucose sanguin est élevé. | VRAI |
| A13. La pyruvate déshydrogénase catalyse la réaction : pyruvate + acétyl-CoA + NAD+ ===> CoA-SH + NADH + H+ + CO2. | FAUX |
| A14. Il y a environ 20 fois plus de glycéraldéhyde 3-phosphate que de dihydroxyacétone phosphate dans la cellule. | FAUX |
| A15. La pyruvate kinase catalyse une réaction qui se déroule au voisinage de l’équilibre. | FAUX |
| A16. Le maltose entre dans la glycolyse sous forme de glucose. | VRAI |
| A17. Il n'existe aucun lien direct entre le pyruvate, l’oxaloacétate et l’acétyl-CoA. | FAUX |
| A18. L’équilibre d’une réaction est atteint quand les concentrations des substrats et des produits sont égales. | FAUX |
| A19. Quand la charge énergétique adénylique est élevée, la glycolyse est activée. | FAUX |
| A20. Certaines enzymes du cycle de Krebs catalysent 2 étapes successives de ce cycle. | VRAI |
| A21. Les sous-unités delta du protéasome 18S possèdent l’activité protéolytique. | FAUX |
| A22. Il y a deux réactions d’oxydo-réduction dans la glycolyse. | FAUX |
| A23. Si le glucose est marqué sur le C1, alors le glycéraldéhyde 3-phosphate est marqué après action de l’aldolase. | FAUX |
| A24. Il existe une corrélation entre l’acide aminé N-terminal et le temps de demi-vie des protéines. | VRAI |
| A25. La réaction catalysée par la lactate déshydrogénase a pour but essentiel de réduire le NADH en aérobiose. | FAUX |
| A26. L’acétyl-CoA est un coenzyme du complexe de la pyruvate déshydrogénase. | FAUX |
| A27. La chaine latérale de K est : -COOH. | FAUX |
| A28. L’ATP est un substrat et un effecteur allostérique de la PFK1. | VRAI |
| A29. La glycolyse ralentit quand la concentration du fructose 2,6 bisphosphate augmente. | FAUX |
| A30. Chez les Eucaryotes, les enzymes du cycle de Krebs sont situées dans l’espace inter-membranaire de la mitochondrie. | FAUX |
| A31. La phosphofructokinase catalyse une réaction d’oxydo-réduction. | FAUX |
| A32. Si Keq = 1, ΔG0' de la réaction = 0. | VRAI |
| A33. Le pyruvate entre dans la matrice mitochondriale par diffusion passive. | FAUX |
| A34. Le coenzyme A est impliqué dans le transfert de groupe glycosyle. | FAUX |
| A35. Le cycle du glyoxylate est spécifique des animaux. | FAUX |
| A36. Le glucose entre et sort librement de la cellule. | VRAI |
A37. La molécule ci-contre est le glucose-1-phosphate. 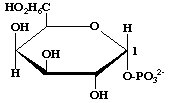 . . |
FAUX |
| A38. La phosphorolyse du glycogène produit le galactose 1-phosphate. | FAUX |
| A39. Le glucose 6-phosphate entre et sort librement de la cellule. | FAUX |
| A40. Les groupes liés au coenzyme A le sont par une liaison thioester. | VRAI |
Question n°2 (10 points) Ecrivez lisiblement la réponse seule - aucun détail de calcul n'est demandé.
Données :
R = 8,31 J.K-1.mol-1
T = 37°C
Trajet optique : l = 1 cm
BSA : εM = 16.000 M-1.cm-1
| Une enzyme catalyse la réaction : A + B <====> C + 2D | |
Q1. La variation d'énergie libre de Gibbs standard de cette réaction vaut : ΔG0' = - 4,7 kJ/mol. Calculez la valeur de la constante d’équilibre Keq. |
Keq = 6,19 |
Q2. In vivo, les concentrations physiologiques des composés sont : [A]φ = 0,01 mM - [B]φ = 360 pM - [C]φ = 3 10-5 M - [D]φ = 2,5 µM. Quelle est la valeur de la constante physiologique Kφ ? |
Kφ = 5,21 10-2 M |
Q3. Calculer ΔG0' de cette réaction. |
ΔG0' = - 12,32 kJ/mol |
| Q4. Si l’on dissout 320 mg de BSA dans 0,2 L, quelle est la concentration molaire de la BSA sachant que sa masse molaire est 6,64 104 g.mol-1 ? | [BSA] = 2,4 10-5 M ou 24 μM |
Q5. Quelle est l’absorbance à 280 nm de 1 mL d’une solution de BSA 120 µM ? |
|